1 רקע על מגיפת הדנגי: אתגר בריאות הציבור העולמי הולך וגובר
דנגי היא מחלה ויראלית חריפה הנישאת על ידי יתושים הנגרמת על ידי נגיף הדנגי (DENV), אשר התגלה כמחלה הארבו-ויראלית המתפשטת במהירות הגבוהה ביותר בעולם, ומהווה איום משמעותי על ביטחון בריאות הציבור. במהלך שני העשורים האחרונים, שכיחות הדנגי העולמית גדלה באופן דרמטי, כאשר מספר המקרים המדווחים הוכפל מדי שנה מאז 2021 [1]. בדצמבר 2023, ארגון הבריאות העולמי (WHO) הכריז על מצב חירום עולמי של דנגי כדי לחזק את מאמצי התגובה הבינלאומיים המתואמים. הערכות אפידמיולוגיות של ארגון הבריאות העולמי מצביעות על כך שכ-3.9 מיליארד אנשים ברחבי העולם נמצאים בסיכון להידבקות בדנגי, כאשר כ-390 מיליון הדבקות מתרחשות מדי שנה - מתוכן 96 מיליון מתבטאים כמקרים גלויים קלינית [1,2].
2 נקודות עיקריות אפידמיולוגיות
המאפיינים האפידמיולוגיים של קדחת הדנגי מעוצבים על ידי האינטראקציה בין גורמים וירולוגיים, אקולוגיה של הווקטורים, תגובות חיסוניות של הפונדקאי ותנאים סוציו-סביבתיים. הבנה מקיפה של מאפיינים אלה חיונית לפיתוח אסטרטגיות מניעה ובקרה יעילות, כמו גם גישות אבחון מדויקות.
2.1 וקטורי תמסורת ודפוסי תמסורת עירוניים
נגיף הדנגי מועבר בעיקר על ידיאדס אגיפטי ואדס אלבופיקטוסיתושים. מבין מיני הווקטורים הללו, Aedes aegypti מוכר כווקטור ההעברה הקריטי ביותר, המאופיין ב"יכולת הסתגלות אנושית" גבוהה ותפוצה נרחבת בסביבות עירוניות טרופיות וסובטרופיות. שלא כמו וקטורים אחרים של יתושים של פתוגנים ארבו-ויראליים, Aedes aegypti מציג את המאפיינים האפידמיולוגיים המרכזיים הבאים:
-העדפה לרבייה בסביבות אנושיות (למשל, מיכלי אחסון מים, צמיגים שהושלכו)
-טרופיזם חזק לדם אנושי כמקור תזונה
-התנהגות אכילה במהלך היום
תכונות אלו מגדירות דנגי כמחלה טיפוסית"מחלה זיהומית עירונית",כאשר יעילות ההעברה עולה משמעותית באזורים צפופי אוכלוסין. מחקרים הקשורים לארגון הבריאות העולמי הראו כי באזורים עירוניים צפופי אוכלוסין, תדירות מוגברת של מגע בין יתושים לבני אדם יכולה להעלות באופן משמעותי את מספר הרבייה הבסיסי (R₀) של DENV, ובכך להאיץ את התפשטות המגיפות [2].
2.2 מגמות התפשטות עולמיות וגורמים מניעים
על פי דיווחי ארגון הבריאות העולמי, מספר מקרי הדנגי המדווחים בעולם גדל באופן אקספוננציאלי בשני העשורים האחרונים [1,3]. מגמת עלייה זו מונעת בעיקר על ידי הגורמים הבאים:
(1) שינויי אקלים: עליית הטמפרטורות הגלובליות לא רק מרחיבה את הטווח הגיאוגרפי של בתי גידול מתאימים לווקטורי יתושים, אלא גם מקצרת את תקופת הדגירה החיצונית של דנגי בתוך הפונדקאי של היתוש, ובכך משפרת את יעילות ההעברה. שינויים בצפיפות היתושים כתוצאה מהאקלים אומתו על ידי ארגון הבריאות העולמי כגורם מנבא אמין לדינמיקה המרחבית-זמנית של התפרצויות דנגי.
(2) עיור: התרחבות עירונית מהירה ולא מתוכננת יצרה בתי גידול רבים עבור וקטורי יתושים, בעוד שצפיפות האוכלוסייה המוגברת חיזקה את המשכיות שרשראות ההדבקה של DENV.
(3) תנועת אוכלוסין עולמית: נסיעות וסחר בינלאומיים אפשרו את ההעברה המהירה חוצת הגבולות של דנגי, וקידמו את המעבר ממקרים מיובאים להעברה מקומית בת קיימא. נתוני מעקב של ארגון הבריאות העולמי מראים כי בין השנים 2010 ו-2021, ארצות הברית דיווחה על 7,528 מקרים של דנגי הקשורים לנסיעות, מתוכם 3,135 הצריכו אשפוז ו-19 גרמו לתמותה.
(4) התפשטות תפוצה וקטורית: ברחבי העולם, הטווח הגיאוגרפי של יתושי Aedes aegypti ו-Aedes albopictus ממשיך להתרחב, כאשר יתושי Aedes מתבססים יותר ויותר בחלקים מאירופה. כתוצאה מכך, קדחת הדנגי התפתחה ממגפה אזורית מסורתית לאיום עולמי על בריאות הציבור.
2.3 מנגנוני מחזור משותף וזיהום חוזר של סרוטיפים מרובים
נגיף הדנגי מורכב מארבעה זנים שונים מבחינה אנטיגנית (DENV-1 עד DENV-4). זיהום בסרוטיפ אחד מקנה חסינות מגנה ארוכת טווח כנגד אותו סרוטיפ ספציפי, אך רק הגנה צולבת זמנית וחלקית כנגד שלושת הסרוטיפים האחרים. האוכלוסייה הכללית רגישה באופן אוניברסלי ל-DENV, כאשר רק תת-קבוצה של אנשים נגועים מפתחת מחלה קלינית [2].
באזורים אנדמיים, מספר זני DENV לעיתים קרובות מסתובבים בו זמנית, מה שמביא לפוטנציאל של אנשים לחוות מספר זיהומים של דנגי במהלך חייהם. מחקרים אפידמיולוגיים של ארגון הבריאות העולמי זיהו מחזור משותף של מספר זני דנגי כגורם מרכזי להתפרצויות דנגי תקופתיות [1].
2.4 זיהום משני והגברה תלוית נוגדנים
תופעה קריטית וייחודית באפידמיולוגיה של דנגי היאהגברה תלוית נוגדנים (ADE)במהלך זיהום משני עם סרוטיפ DENV הטרולוגי, נוגדנים שאינם מנטרלים המיוצרים במהלך הזיהום הראשוני מקלים על כניסת הנגיף למונוציטים ולמקרופאגים, ובכך משפרים את שכפול הנגיף. מנגנון זה מוכר באופן נרחב על ידי ארגון הבריאות העולמי כגורם פתוגני עיקרי בקדחת דנגי קשה, כולל קדחת דימומית דנגי ותסמונת הלם דנגי [1].
נתונים אפידמיולוגיים של ארגון הבריאות העולמי מראים באופן עקבי כי אנשים עם זיהום דנגי משני נמצאים בסיכון גבוה משמעותית לפתח מחלה קשה בהשוואה לאלו עם זיהום ראשוני - מאפיין בעל חשיבות רבה למעקב אחר המחלה ולניהול הקליני. חשוב לציין כי בעוד שהסיכון למחלה קשה עולה במהלך זיהום משני, זיהום בכל סרוטיפ DENV יכול להתקדם לדנגי חמור [1].
2.5 תופעות קליניות לא ספציפיות וסיכון לאבחון שגוי
הביטויים הקליניים של קדחת דנגי אינם ספציפיים באופן בולט, במיוחד בשלבים המוקדמים של המחלה, ולעתים קרובות חופפים לאלו של זיהומים ויראליים אחרים הנישאים על ידי יתושים (למשל, נגיפי צ'יקונגוניה וזיקה) כמו גם לזיהומים בדרכי הנשימה מסוימים. הערכות ארגון הבריאות העולמי מצביעות על כך ש-40-80% מזיהומי דנגי הם אסימפטומטיים [3].
ביטויים קליניים אופייניים כוללים:
חום חריף (נמשך 2-7 ימים, ויכול להיות דו-פאזי)
כאב ראש חמור וכאב אחורי (כאב מאחורי העיניים)
כאבי שרירים ומפרקים (המכונים בדרך כלל "קדחת שבירת עצם")
פריחה מקולרית או מקולופפולרית
-תופעות דימומיות קלות (למשל, אקכימוזיס, אפיסטקסיס, דימום חניכיים)
קדחת דנגי סימפטומטית מחולקת בדרך כלל לשלושה שלבים נפרדים: שלב החום, השלב הקריטי ושלב ההחלמה. פחות מ-5% מהחולים הסימפטומטיים מתקדמים לקדחת דנגי חמורה. בשל היעדר מאפיינים קליניים ספציפיים, אבחון המבוסס אך ורק על תסמינים קליניים הוא מאתגר, מה שמגביר את הסיכון לאבחון שגוי ותת-אבחון. ארגון הבריאות העולמי מדגיש במפורש כי אבחון קליני לבדו אינו מספיק כדי להבטיח דיוק, מה שהופך את אישור המעבדה לחיוני [1].
3 נקודות מפתח מ"בדיקות מעבדה לנגיף דנגי: הנחיות ביניים, אפריל 2025" של ארגון הבריאות העולמי
באפריל 2025, פרסם ארגון הבריאות העולמי הנחיות ביניים מעודכנות בנוגע לבדיקות מעבדה ל-DENV, המספקות הנחיות טכניות מוסמכות לאבחון דנגי עולמי. הנחיות אלו מסנתזות את הראיות העדכניות ביותר בנוגע לבדיקות מעבדה לדנגי בהקשר של מצב החירום העולמי המתמשך של דנגי ומציעות המלצות מעשיות המותאמות למסגרות עם רמות משאבים משתנות.

3.1 עקרונות יסוד של אסטרטגיית בדיקה
ההנחיות מדגישות כי אבחון קדחת הדנגי חייב לאמץ אסטרטגיית בדיקה משולבת מרובת סמנים המבוססת על שלב המחלה [1]. בהיעדר אלגוריתם אבחון אוניברסלי, יש להתאים את אסטרטגיות הבדיקה להקשרים אפידמיולוגיים מקומיים, תוך התחשבות בגורמים המרכזיים הבאים [1]:
שלב ההדבקה: מספר הימים לאחר הופעת התסמין קובע את שיטת הבדיקה המתאימה ביותר.
סוג הדגימה: התאמת דם מלא, פלזמה או סרום לגילוי DENV
אפידמיולוגיה אזורית: סרוטיפים מקומיים של DENV ומחזור משותף של ארבו-וירוסים אחרים
סיכון לזיהום משותף: באזורים עם מחזור חופף של ארבו-וירוס, יש לשקול בדיקות מרובות כדי להבחין בין פתוגנים שונים.
3.2 אסטרטגיית בדיקה מבוססת שלבים
על פי הנחיות ארגון הבריאות העולמי, בדיקות מעבדה לקדחת דנגי צריכות לעקוב אחר חלונות זמן ברורים המבוססים על שלב המחלה [1,2]:
(1) בדיקת פאזה חריפה (≤7 ימים לאחר הופעת המחלה)
בדיקת חומצות גרעין (בדיקה מולקולרית): תגובת שרשרת פולימראזית הפוך (RT-PCR) ושיטות מולקולריות אחרות מזהות RNA של DENV ברגישות גבוהה.
בדיקת אנטיגן: גילוי אנטיגן NS1, אשר הופך לזיהוי תוך 1-3 ימים לאחר הופעת המחלה.
במהלך השלב האקוטי, רמות הווירמיה גבוהות יחסית, ובדיקות חומצות גרעין ואנטיגן משיגות רגישות אופטימלית.
(2) בדיקת שלב ההחלמה (4 ימים ומעלה לאחר תחילת המחלה)
בדיקה סרולוגית: נוגדנים ל-IgM ניתנים לזיהוי בדרך כלל בסביבות היום הרביעי לאחר הופעת המחלה.
ברוב המקרים, נוגדני IgM נמשכים 14-20 ימים, ובמקרים מסוימים, ההישרדות יכולה להימשך עד 90 ימים.
לבדיקת IgG ערך מוגבל לאבחון דנגי חריף עקב נוגדנים צולבים פוטנציאליים מזיהום קודם של נגיף פלביו או חיסון.
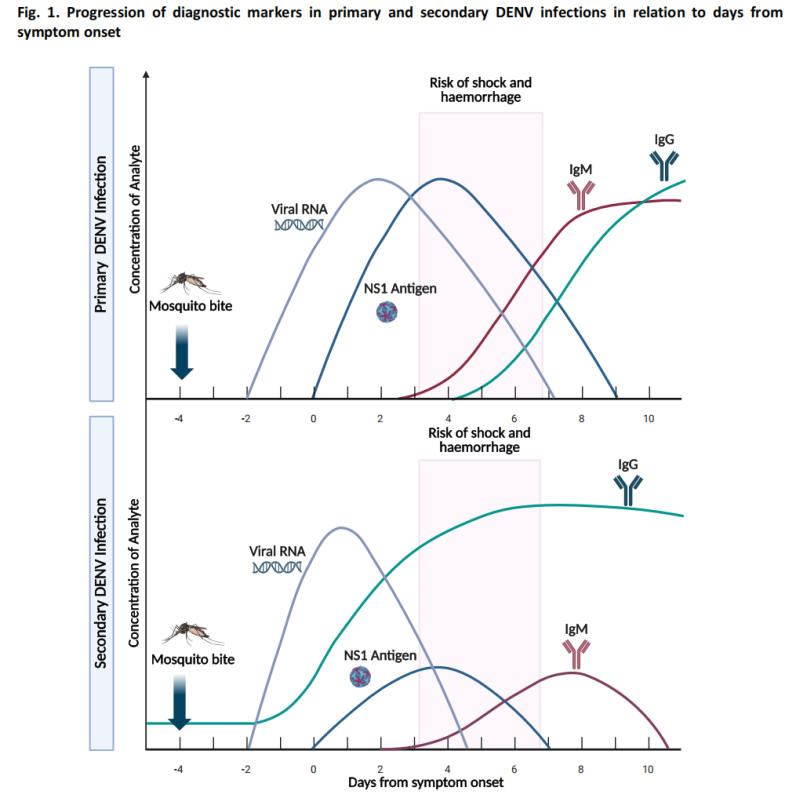
(3) אלגוריתם אבחון מקרים חשודים
ההנחיות כוללות אלגוריתם אבחוני למקרים חשודים של קדחת דנגי, וממליצות על שיטות בדיקה מתאימות המבוססות על ימים לאחר הופעת התסמין: בדיקת אנטיגן NS1 ובדיקת חומצות גרעין הן הגישות העיקריות בשלב המוקדם, בעוד שבדיקות סרולוגיות הן השיטה העיקרית בשלב המאוחר.
3.3 הערכת ביצועי שיטת הבדיקה ובחירתה
על פי ארגון הבריאות העולמי, הערכה שיטתית של הביצועים והתרחישים הרלוונטיים של בדיקות דנגי שונות היא כדלקמן:
| שיטת בדיקה | יַעַד | חלון זמן | תרחיש יישום ראשי | שיקולים |
| בדיקת חומצות גרעין | RNA ויראלי | 1-7 ימים לאחר הופעת המחלה | אימות מוקדם, זיהוי סרוטיפ | שיטת תקן הזהב; דורשת ציוד מעבדה מיוחד ומומחיות טכנית |
| בדיקת אנטיגן NS1 | חלבון לא מבני | 1-3 ימים לאחר הופעת המחלה | סינון מהיר מוקדם | זמין בפורמט בדיקת אבחון מהירה (RDT), מתאים למסגרות עם משאבים מוגבלים |
| בדיקת נוגדנים מסוג IgM | נוגדנים ספציפיים ל-IgM | ≥4 ימים לאחר הופעת המחלה | אבחון של זיהום אחרון | דגימת סרום בודדת רק מצביעה על זיהום אפשרי לאחרונה; נדרשת סרוקונברסיה לאישור |
| בדיקת נוגדנים מסוג IgG | נוגדנים ספציפיים של IgG | זיהום קודם/בהחלמה | חקירה אפידמיולוגית, הערכת מצב חסינות | דגימת סרום בודדת אינה מתאימה לאבחון דנגי חריף |
| בדיקה משולבת (NS1+IgM/IgG) | אנטיגן + נוגדנים | מהלך מחלה מלא | אבחון מקיף של זיהום דנגי | נכון לעכשיו, פורמט ה-RDT בעל הביצועים הטובים ביותר לאבחון דנגי |
| NGS | RNA ויראלי | 1-7 ימים לאחר הופעת המחלה | מעקב גנומי ויראלי | דורש ציוד ריצוף מיוחד ויכולות ניתוח ביואינפורמטיקה |
4 המלצות למוצרי גילוי דנגי בבדיקות מאקרו ומיקרו לפי תרחיש
כדי לתמוך במניעה ובשליטה של קדחת דנגי, Macro & Micro-Test מספקת תיק אבחונים משולב הכולל סינון מהיר, אישור מולקולרי ומעקב גנומי, ועונה על צרכים בשלבי ניהול שונים של התפרצות.
4.1 תרחיש 1: סינון מהיר ומעקב ממוקד
חל על מרפאות חום, מתקני בריאות ראשוניים, בדיקות סקר קהילתיות להתפרצויות ובידוד בנמלים/גבולות.
בדיקת מהירה לאנטיגן NS1 של נגיף דנגי: מזהה זיהום מוקדם (1-3 ימים לאחר הופעת המחלה) עם תוצאות תוך 15 דקות לצורך מיון מהיר.
בדיקת נוגדנים IgM/IgG לנגיף דנגי: מבחינה בין זיהומים ראשוניים ומשניים כדי להעריך את הסיכון למחלה חמורה.
בדיקה מהירה משולבת של אנטיגן NS1 לנגיף דנגי + IgM/IgG: מזהה בו זמנית אנטיגן ונוגדנים לאבחון מלא.
בדיקת נוגדנים IgM/IgG לנגיף צ'יקונגוניה: מאפשרת אבחנה מבדלת עם דנגי לזיהוי מדויק של פתוגנים.
4.2 תרחיש 2: אבחון מדויק ותגובה לחירום
ערכת גילוי חומצות גרעין לנגיף דנגי I/II/III/IV: מזהה ומבדילה בין 4 זנים שונים (סף גילוי 500 עותקים/מ"ל) לצורך מעקב אחר התפרצות.
ערכת PCR ליופיליזציה של נגיף דנגי: ניתנת להובלה בטמפרטורת החדר, מתאימה לאזורים מוגבלים במשאבים ולהתפרצויות פתאומיות.
ערכת PCR בזמן אמת לדנגי/זיקה/צ'יקונגוניה: מזהה בו זמנית 3 ארבו-וירוסים לאבחון דיפרנציאלי יעיל בהתפרצויות מורכבות.

כל הריאגנטים הנ"ל תואמים למערכת AIO 800 אוטומטית לחלוטין מדגם לתשובה, מה שמפחית את הפעולה הידנית והזיהום הצולב, ומשפר את היעילות והבטיחות הביולוגית.
4.3 תרחיש 3: מעקב גנומי וניתוח שושלת ויראלית
ישים למעבדות ייחוס לאומיות, מוסדות מחקר לבריאות הציבור, בהתאם לעמדת ארגון הבריאות העולמי לגבי NGS.
פתרונות המעקב הגנומי של Macro & Micro-Test תומכים בריצוף גנום שלם לצורך איתור וירוסים, בירור שרשרת הדבקה, ניטור וריאנטים והתאמת אסטרטגיית חיסון. הם תומכים בזרימות עבודה ידניות/אוטומטיות, משפרים את התפוקה ואת יכולת השחזור, ומאפשרים למעבדות לשדרג מבדיקות שגרתיות למעקב מתקדם, בהתאם לדגש של ארגון הבריאות העולמי על חיזוק ניטור האבולוציה הנגיפית.

4.4 ערך הפתרונות המשולבים
Macro & Micro-Test מספקת פתרונות אבחון מלאים לגילוי ארבו-וירוס, התומכים בכל שלב בניהול התפרצות: כלי סינון מהירים עבור מערכות שירותי בריאות בחזית, אישור מולקולרי לאבחון מדויק ויכולות ניתוח גנום שלם למעקב אפידמיולוגי. עם בדיקות בעלות ביצועים גבוהים, זרימות עבודה גמישות ופלטפורמות מוכנות לאוטומציה, פתרונות אלה מעצימים מעבדות ומערכות בריאות הציבור לחזק את המוכנות והתגובה לאיומי ארבו-וירוס מתעוררים ברחבי העולם.
הפניות
[1] ארגון הבריאות העולמי. בדיקות מעבדה לנגיף דנגי: הנחיות ביניים, אפריל 2025. ז'נבה: ארגון הבריאות העולמי; 2025.
[2] קבוצת הייעוץ הטכנית של יוזמת הארבו-וירוס העולמית של ארגון הבריאות העולמי. חיזוק המוכנות והתגובה העולמית לאיומי מחלות ארבו-וירוסיות: קריאה לפעולה. Lancet Infect Dis. 2026;26(1):15-17.
[3] חיידק הלנסט. התגברות על הדילמה של אבחון דנגי. חיידק הלנסט. 2025;6(7):101190.
זמן פרסום: 20 במרץ 2026
